
近期,西南大学药学院中医药学院李翀教授团队、澳门科技大学姜志宏教授团队在Nature Communications(IF=14.7)上发表题为“Berberine-inspired ionizable lipid for self-structure stabilization and brain targeting delivery of nucleic acid therapeutics.(小檗碱激发的离子化脂质用于核酸治疗的自我结构稳定化及脑靶向递送)”的研究。该研究基于天然小檗碱的分子特性,创新设计出多功能脂质纳米载体,成功突破血脑屏障递药难题,为阿尔茨海默病等中枢神经系统疾病的基因治疗提供了全新解决方案。
欣博盛生物非常荣幸能够作为供应商为该项研究提供高品质ELISA试剂盒,为生物医学领域的科研探索贡献一份力量。
引用产品
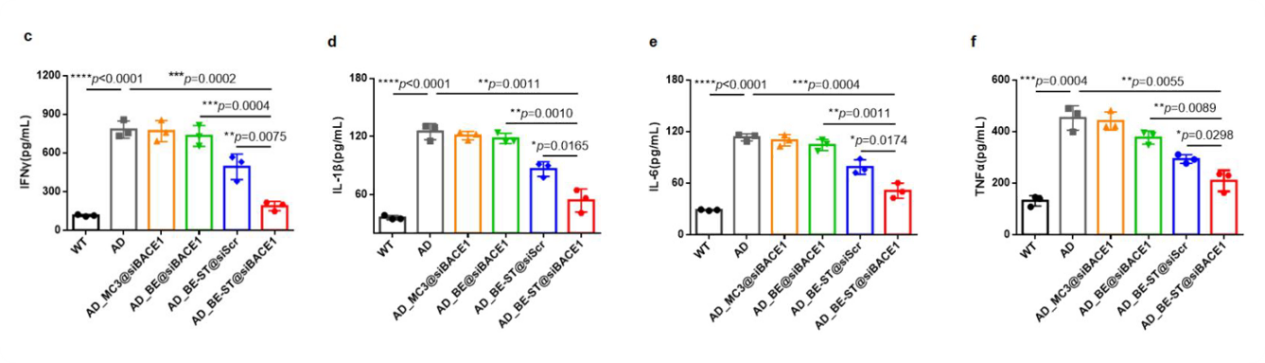
该项研究中,使用了欣博盛生物(NeoBioscience Technology Co, Ltd)的Mouse IL-1β, IL-6, IFN-γ and TNF-α ELISA Kit,用于检测小鼠血浆样本中相关炎症因子指标,以了解LNP@siBACE1对阿尔茨海默病(AD)的协同影响。
货号 | 产品名称 | 灵敏度 | 检测范围 |
EMC001b | QuantiCyto® Mouse IL-1β ELISA kit (小鼠白细胞介素-1β) | 7.8pg/ml | 15.6-1000pg/ml |
QuantiCyto® Mouse IL-6 ELISA kit (小鼠白细胞介素-6) | 7.8pg/ml | 15.6-1000pg/ml | |
QuantiCyto® Mouse IFN-γ ELISA kit (小鼠γ干扰素) | 3.9pg/ml | 7.8-500pg/ml | |
QuantiCyto® Mouse TNF-α ELISA kit (小鼠肿瘤坏死因子-α) | 15.6pg/ml | 31.25-2000pg/ml |
研究详情
血脑屏障(blood-brain barrier, BBB)是保护大脑的“天然防线”,同时却也让98%的药物难以进入脑组织;同时,核酸药物易降解、稳定性差,进一步限制了基因疗法的应用。传统脂质纳米粒(lipid nanoparticles, LNP)依赖静电作用携载药物,存在靶向性低、稳定性不足等问题。如何实现“精准穿透屏障+高效保护药物”的双重目标?李翀教授团队给出了创新答案,提出了一系列受小檗碱生物碱结构激发的离子化脂质,从分子层面到动物研究层面全面验证揭示了第二代生物碱基LNP的关键优势。
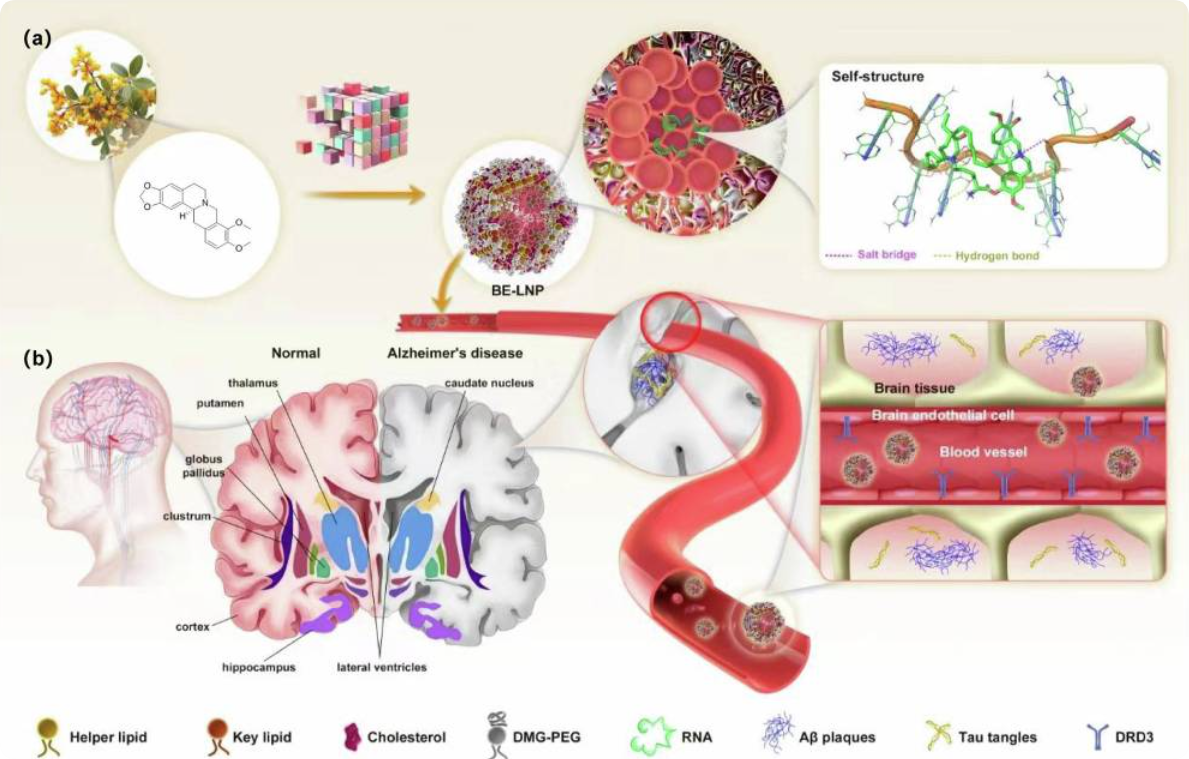
(小檗碱仿生脂质载体靶向脑递送的设计和机制)

(BE脂质体分子开发的优化流程)
创新突破:天然小檗碱赋能“三位一体”递送系统
稳定自结构:载体骨架通过氢键与核酸药物高效结合,携载能力提升2倍以上;
智能靶向穿透:天然亲和多巴胺D3受体,驱动血脑屏障高效跨膜(体外靶向效率提升65倍,脑-肝分布比达20%);
协同治疗活性:保留小檗碱抗炎、抗氧化特性,直击脑部疾病微环境。
疗效验证:多疾病模型展现卓越潜力
阿尔茨海默病治疗
研究团队使用阿尔茨海默病(AD)小鼠模型评估了BE-ST递送系统(BE+Scutellarin)靶向BACE1的效果。APP/PS1小鼠接受BE-ST@siBACE1处理后,在Morris水迷宫测试中表现出显著的认知功能改善,表现为在目标象限停留时间延长1.95倍,穿越目标象限次数增加。同时,BE-ST@siBACE1处理显著降低了海马和皮层中BACE1的水平,减少了海马、皮层和血清中的淀粉样斑块数量和大小,并降低了海马和皮层中的过度磷酸化tau蛋白(p-tau)水平。这些结果表明BE-ST递送系统在AD治疗中具有潜在的应用价值。
脑胶质瘤治疗
研究团队评估了BE-ST递送系统在多种病理模型中的多功能性,使用GL261-Luc脑肿瘤小鼠模型评估了siVEGF的递送效果。数据表明,BE-ST处理显著降低了脑肿瘤的平均荧光强度(MFI),病灶荧光强度于给药后第3天降低27.96%,于第6天降低38.82%,证实了BE-ST在病灶部位的靶向能力增强。
隐球菌性脑膜炎治疗
通过评估AMB负载的LNPs,发现BE-ST@AMB显著增强了AMB的递送和疗效,治疗后脑部荧光信号大幅降低,小鼠生存率得到了显著的提高。
综上所述,本研究突破传统设计,创新开发出基于四氢异喹啉双稠环骨架的可电离脂质,实现核酸高效装载及内涵体逃逸。该脂质纳米粒兼具抗氧化/抗炎特性,可缓解RNA制剂的免疫原性,并凭借小分子配体特性突破血脑屏障,递送效率显著优于传统靶向方法。其特有的脑血流调控能力实现"主动分布-精准靶向"双重效应,为siRNA/mRNA等中枢神经递送开辟新途径,为神经退行性疾病治疗提供了新的方案。
该研究由西南大学药学院中医药学院为第一完成单位,博士研究生边煦霏、郭倩为共同第一作者,李翀教授与澳门科技大学姜志宏教授为共同通讯作者。研究获国家重点研发计划、国家自然科学基金、重庆市杰出青年科学基金等资金支持。
文献引用
Bian X, Guo Q, Yau L F, et al. Berberine-inspired ionizable lipid for self-structure stabilization and brain targeting delivery of nucleic acid therapeutics[J]. Nature Communications, 2025, 16(1): 2368.


